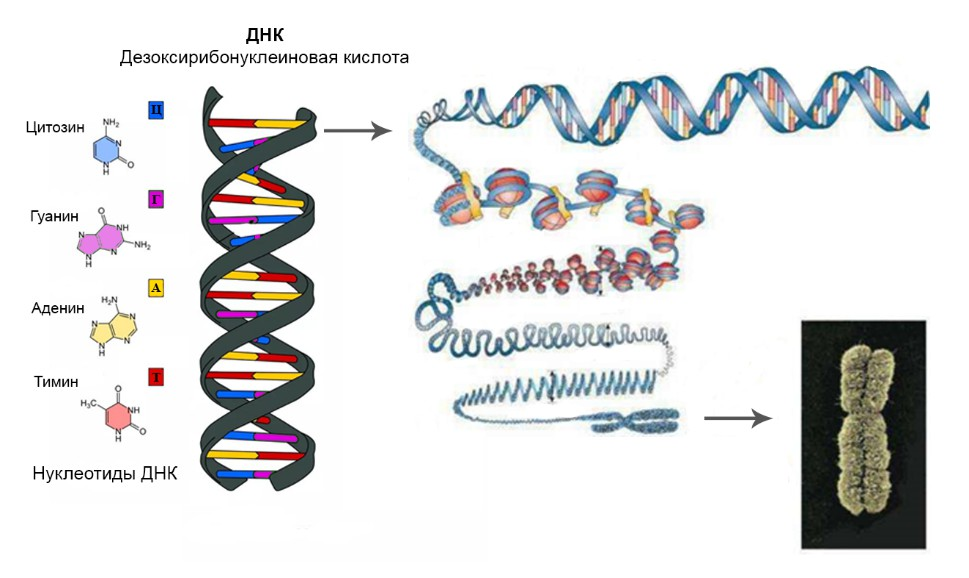
Наш организм хранит практически всю информацию о себе в молекулах ДНК — длинных цепочках, закодированных с помощью четырех «букв» — аденина (А), тимина (Т), цитозина (Ц) и гуанина (Г). Эти «буквы» образуют последовательности, которые определяют структуру и функции всех белков, отвечающих за работу нашего организма. ДНК очень сильно сжата и хранится в виде хромосом. Маленькие участки ДНК, называемые генами, содержат инструкции для синтеза этих белков. Именно изменения в генах — мутации — могут стать причиной развития заболеваний.
Мутации в генах могут передаваться из поколения в поколение и приводить к различным наследственным заболеваниям. Именно с этим работают специалисты лаборатории генной инженерии НМИЦ гематологии Минздрава России, проводя генетическое тестирование.
Подробнее о том, как генетическое тестирование помогает выявить наличие мутаций и оценить их влияние на здоровье человека рассказала заведующая лабораторией Олеся Пшеничникова.
— Например, мутации в некоторых генах могут вызывать такие заболевания, как наследственная глухота, гемофилия или болезнь Гоше. Зная о них заранее, можно вовремя начать лечение и минимизировать развитие симптомов. Проведение генетического тестирования для всех членов семьи с наследственным заболеванием имеет ряд важных преимуществ, которые помогают улучшить качество жизни и здоровье.
Генетическое тестирование полезно не только для постановки диагноза, но и для предупреждения осложнений или корректного выбора терапии. Примером может служить тромботическая тромбоцитопеническая пурпура: зная, наследственная она или приобретенная, врачи могут выбрать соответствующее лечение. Генетическое тестирование также важно при подозрении на порфирию, так как только оно может подтвердить диагноз. Кроме того, выявление носителей мутаций среди родственников пациентов с порфирией позволяет им избегать факторов риска и минимизировать вероятность развития заболевания. А диагностика наследственных коагулопатий у женщин позволяет врачам правильно вести беременность и предотвратить осложнения во время родов. Выявление мутаций в таких генах, как MYH9, которые с возрастом могут приводить к нарушениям в разных системах органов, позволяет проводить регулярный мониторинг и вовремя принять превентивные меры. В случае тяжелых гематологических заболеваний, таких как гемофилия или бета-талассемия, выявление мутаций и определение статуса носительства помогает принимать взвешенные решения при планировании семьи.
Генетическое тестирование начинается с консультации у врача-генетика, который изучает историю болезни пациента и его семьи, объясняет процесс тестирования. Затем пациент сдает биоматериал — обычно это венозная кровь. Из нее в лаборатории выделяют ДНК и и проводят генетическое исследование. Результаты теста врач-генетик подробно объясняет, после чего дает рекомендации по дальнейшим шагам.
Процесс исследования начинается с выделения ДНК из клеток крови. В качестве материала чаще всего выступает венозная кровь, взятая с антикоагулянтом ЭДТА, который предотвращает ее преждевременное свертывание. В настоящее время существует много различных вариантов выделения ДНК, все они заключаются в том, что ядерные клетки, в случае крови – это лейкоциты, лопаются, и ДНК из них выходит наружу, в пробирку, где она осаждается специальными методами и отмывается от всего лишнего. В итоге получается осадок из ДНК, который затем растворяют в воде или специальном буфере. После этого ДНК готова к дальнейшей работе. Далее мы увеличиваем количество копий интересующего нас фрагмента ДНК с помощью метода полимеразной цепной реакции (ПЦР). Этот метод позволяет нам получить большое количество копий фрагмента и повысить чувствительность теста. Чтобы убедиться, что все прошло правильно, мы используем метод электрофореза, который позволяет визуализировать фрагменты ДНК под действием ультрафиолетового света и проверить, получен ли нужный результат.
Далее следует секвенирование ДНК по методу Сэнгера, чтобы определить точную последовательность нуклеотидов. Полученные данные сравниваются с референсной последовательностью на предмет поиска отличий, и наши специалисты на основе различных баз данных анализируют, могут ли выявленные изменения быть причиной заболевания. Анализ данных является самой важной частью диагностики и требует высокой квалификации специалистов.
Типы наследования генетических заболеваний: что нужно знать?
Понимание типов наследования генетических заболеваний помогает предсказать вероятность того, что ребенок унаследует ту или иную патологию от родителей. Тип наследования зависит от двух факторов: на какой хромосоме находится ген, изменения в котором вызывают болезнь, и сколько копий гена должно быть повреждено, чтобы заболевание проявилось. Эти факторы могут встречаться в различных комбинациях.
Если ген, вызывающий заболевание, расположен на одной из неполовых хромосом (аутосом), то мы говорим об аутосомном наследовании. Если он находится на половых хромосомах (Х или Y), это сцепленное с полом наследование.
Когда заболевание развивается из-за повреждения только одной копии гена, это называется доминантным наследованием. Если же болезнь проявляется только при наличии двух поврежденных копий гена, речь идет о рецессивном наследовании.
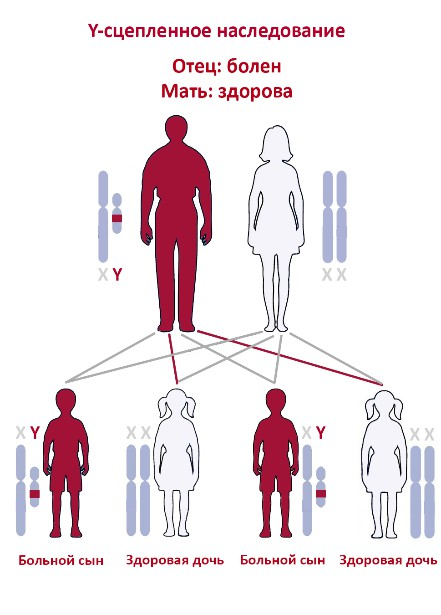
Y-сцепленное наследование
При Y-сцепленном наследовании заболевание вызывается нарушениями в генах, расположенных на Y-хромосоме, и передается только от отца к сыну, так как только мужчины имеют Y-хромосому. Женщины и их потомки не будут болеть. Одним из примеров является пигментный ретинит — заболевание, приводящее к прогрессирующему ухудшению зрения и слепоте.
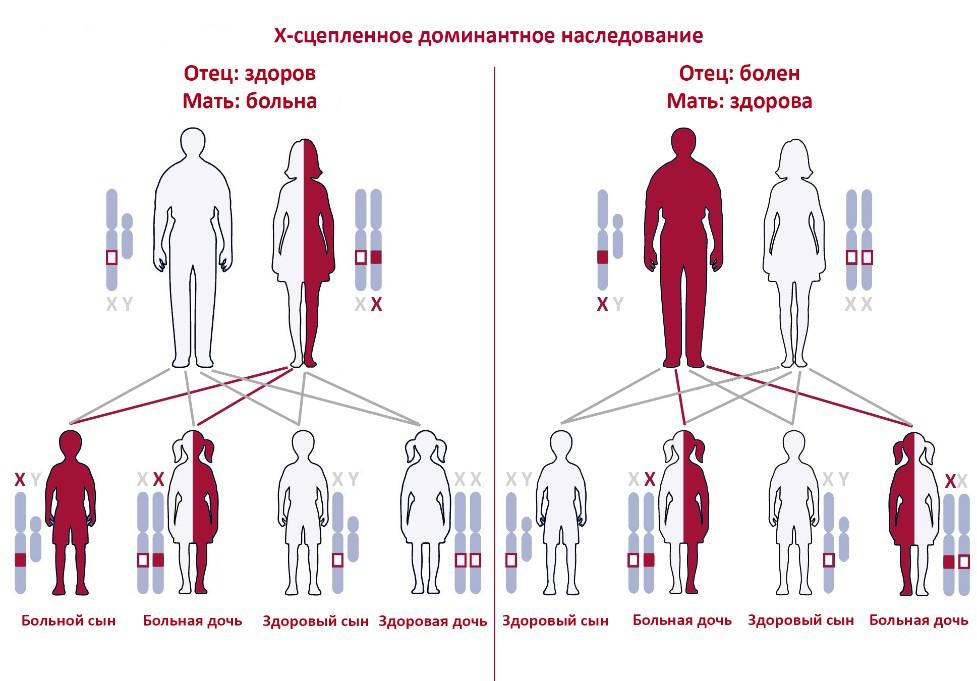
Х-сцепленное наследование
Мутации в генах, расположенных на Х-хромосоме, могут вызывать Х-сцепленные болезни. При Х-сцепленном доминантном наследовании заболевание может проявиться как у женщин, так и у мужчин, но мужчины передают мутацию только своим дочерям. Вероятность передачи болезни ребенку составляет 50%. Примером такого заболевания является крайне редкий тип порфирии — Х-сцепленная протопорфирия. Это заболевание вызвано нарушением в одном из ферментов, участвующих в биосинтезе гема, компонента гемоглобина и некоторых других белков, характеризующееся повышенной чувствительностью к солнечному свету.
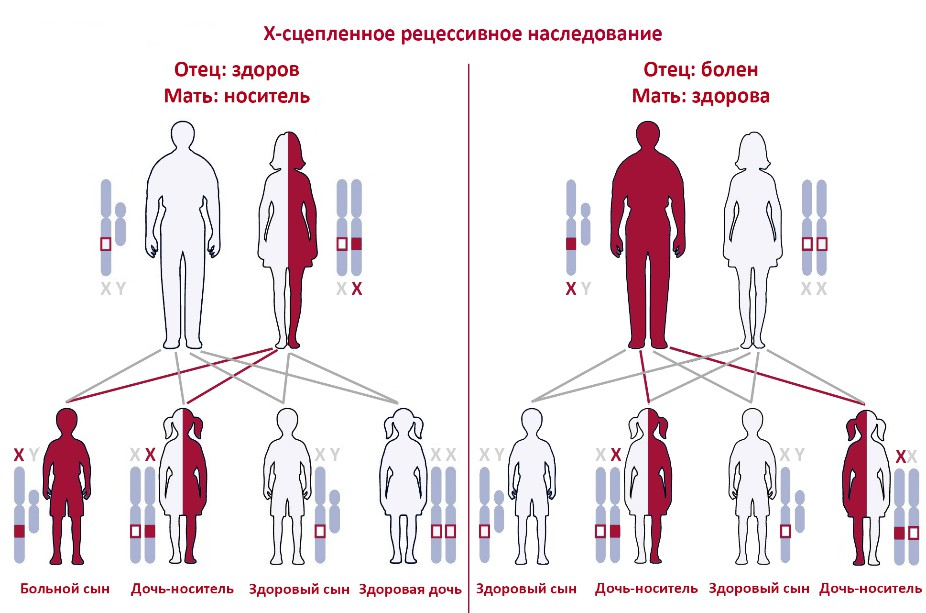
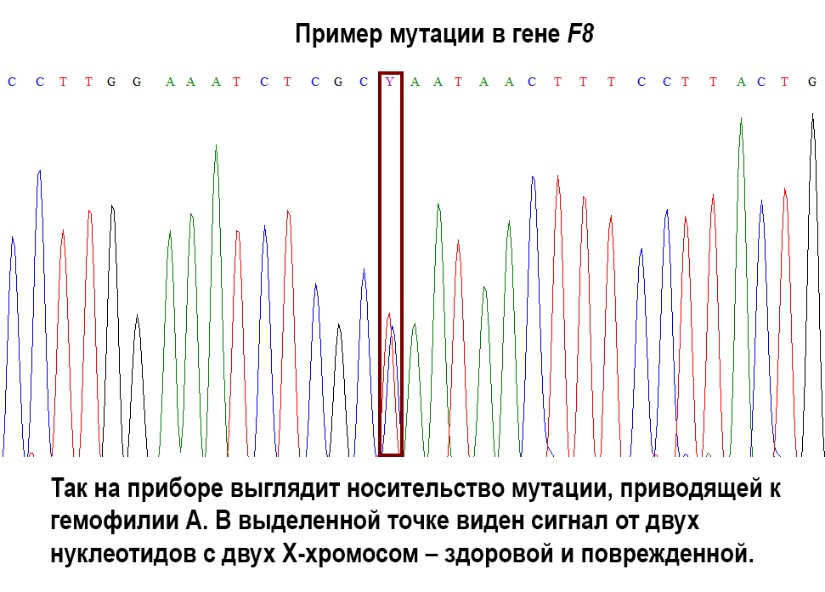
Х-сцепленное рецессивное наследование чаще всего затрагивает мужчин, поскольку они имеют только одну Х-хромосому. Женщины обычно являются бессимптомными носителями и заболевают только в случае, если обе их Х-хромосомы несут мутантный вариант гена, или если здоровая Х-хромосома по каким-то причинам не функционирует. Все дочери больного мужчины будут бессимптомными носителями, все сыновья здоровыми. Дети от женщины-носительницы унаследуют ген с мутацией с вероятностью 50%. Примером такого заболевания является гемофилия — нарушение свертываемости крови. Мужчины болеют гемофилией, если унаследуют ген F8 с мутацией от матери-носительницы.
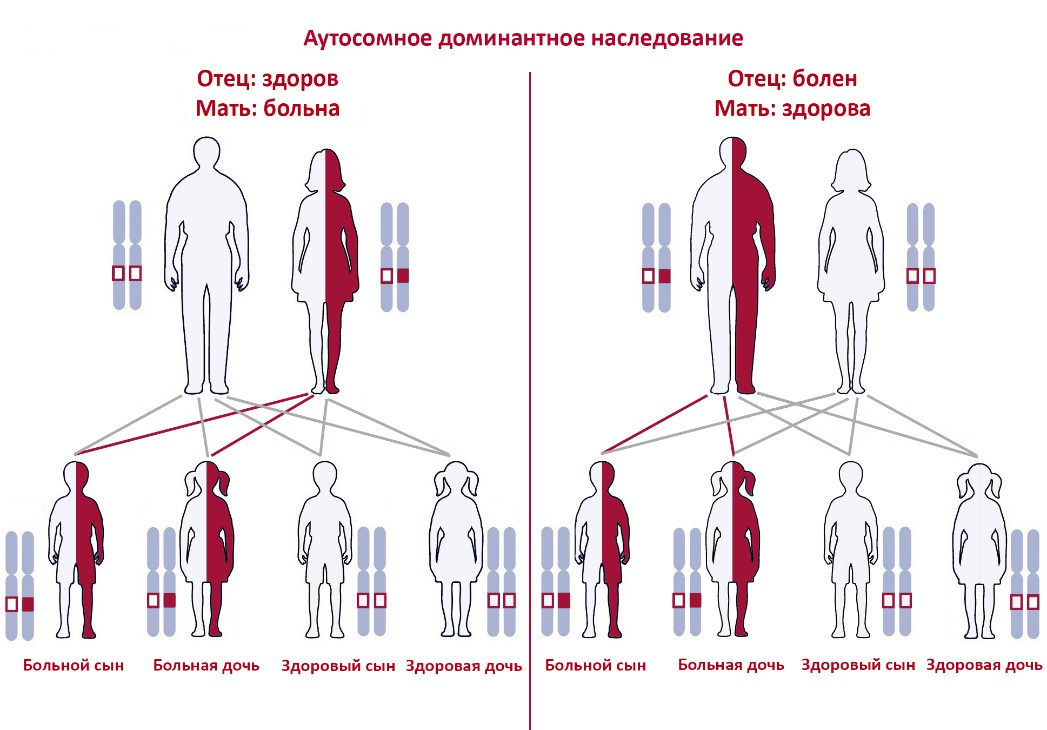
Аутосомно-доминантное наследование
При аутосомно-доминантном наследовании заболевание развивается, если повреждена хотя бы одна копия гена. Один из родителей часто также болен и может передать мутацию ребенку с вероятностью 50%. Примером такого типа наследования является острая перемежающаяся порфирия — заболевание, связанное с нарушением синтеза гема, что вызывает накопление токсичных веществ и приводит к симптомам, таким как боли в животе и паралич.
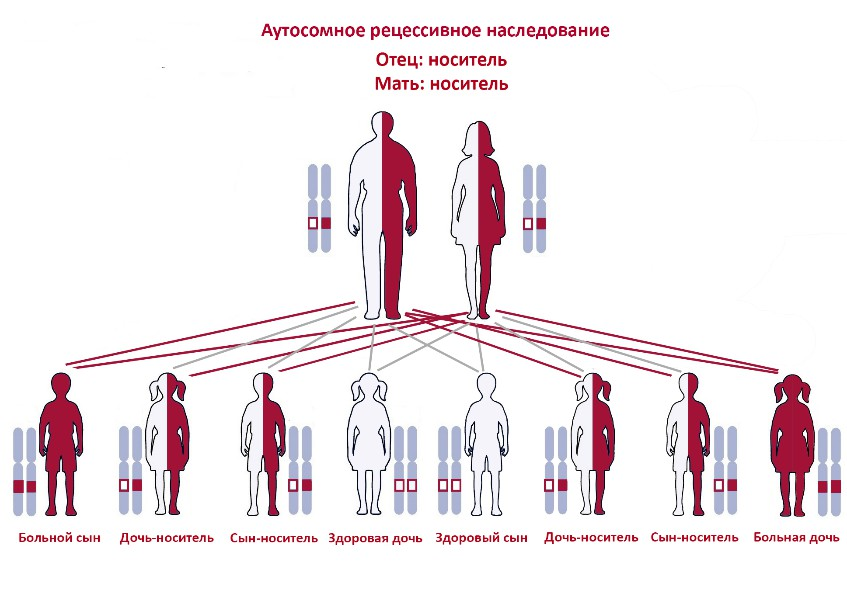
Аутосомно-рецессивное наследование
В случае аутосомно-рецессивного наследования заболевание проявляется, если человек унаследовал две мутантные копии гена — одну от каждого родителя. Родители при этом могут быть носителями и не иметь симптомов. Вероятность рождения больного ребенка у двух носителей составляет 25%. Примером является тяжелая форма бета-талассемии — тяжелого заболевания, связанного с нарушением синтеза гемоглобина, которое приводит к анемии и требует регулярных переливаний крови.
Знание типа наследования важно для понимания риска передачи заболевания и планирования семьи, особенно в случаях, когда наследственные болезни могут серьезно повлиять на здоровье. Однако необходимо учитывать, что иногда мутации могут возникать спонтанно в половых клетках родителей.
Пренатальная диагностика наследственных заболеваний
Пренатальная диагностика — это комплекс методов, которые позволяют выявить генетические заболевания и врожденные аномалии у плода до его рождения. Эти исследования помогают будущим родителям узнать о возможных рисках и принимать взвешенные решения.
Инвазивные и неинвазивные методы пренатальной диагностики
Пренатальная диагностика делится на инвазивные и неинвазивные методы. Неинвазивные методы не требуют проникновения в полость матки, что делает их более безопасными. Самый распространенный неинвазивный метод — это неинвазивное пренатальное тестирование (НИПТ). Он основан на анализе ДНК плода, выделенной из крови беременной женщины. Этот тест позволяет определить пол ребенка и выявить некоторые генетические патологии на ранних сроках беременности.
Однако для более точной диагностики часто применяют инвазивные методы, которые дают возможность получить образцы тканей плода или плаценты. Эти методы позволяют собрать больше данных о генетических нарушениях, хотя они связаны с некоторыми рисками. К инвазивным методам относятся биопсия хориона, амниоцентез, биопсия плаценты и кордоцентез.
-
Биопсия хориона проводится на сроке 10-12 недель беременности. В ходе этой процедуры берется образец ткани плаценты, содержащей клетки плода, из которых выделяют ДНК для анализа. Этот метод помогает выявить генетические аномалии на ранних этапах беременности, давая родителям возможность принять решение о дальнейших шагах на безопасном сроке.
-
Амниоцентез выполняется на сроке 15-20 недель и включает забор амниотической жидкости, которая содержит клетки плода. Этот метод может выявить широкий спектр генетических нарушений и аномалий развития. Также амниоцентез позволяет оценить состояние плода, определить наличие гипоксии, оценить степень развития плаценты и выявить резус-конфликт между матерью и ребенком.
-
Плацентоцентез и кордоцентез выполняются после 18 недели беременности. При плацентоцентезе анализируется ДНК из ткани плаценты, а при кордоцентезе — из пуповинной крови плода. Эти методы используются для подтверждения диагнозов и более детального изучения выявленных аномалий.
Хотя инвазивные методы связаны с незначительным риском осложнений (например, угроза выкидыша, инфекция или кровотечение), современные медицинские технологии позволяют свести эти риски к минимуму. Вероятность осложнений составляет менее 1%.
Пренатальная диагностика — это важный инструмент, который помогает выявить генетические патологии на ранних сроках беременности. Она дает будущим родителям возможность лучше подготовиться к возможным медицинским вызовам, планировать специализированную помощь для ребенка и принимать взвешенные решения о продолжении беременности.
Генетическое тестирование при экстракорпоральном оплодотворении
Экстракорпоральное оплодотворение (ЭКО) — это метод вспомогательной репродуктивной технологии, при котором оплодотворение яйцеклетки сперматозоидом происходит вне тела женщины, в лабораторных условиях. После оплодотворения эмбрион, начавший делиться, переносится в полость матки для дальнейшего развития. Важным этапом процедуры ЭКО является генетическое тестирование эмбрионов, которое позволяет выявить генетические аномалии еще до их переноса в матку. Это значительно повышает вероятность успешной беременности и рождения здорового ребенка.
Генетическое тестирование эмбрионов помогает определить их генетическую нормальность, что увеличивает шансы на успешную имплантацию и вынашивание беременности. Кроме того, это позволяет избежать передачи серьезных наследственных заболеваний будущему поколению.
Существует несколько методов генетического тестирования эмбрионов, применяемых в рамках ЭКО:
-
Преимплантационное генетическое тестирование анеуплоидий (ПГТ-А) позволяет выявить хромосомные аномалии, такие как синдром Дауна, синдром Эдвардса и синдром Патау. Эти отклонения связаны с изменением числа хромосом у эмбриона.
-
Преимплантационное генетическое тестирование моногенных заболеваний (ПГТ-М) используется для выявления конкретных мутаций, которые передаются в семье. Это особенно актуально для семей с историей таких заболеваний, как гемофилия, муковисцидоз или бета-талассемия.
-
Преимплантационное генетическое тестирование структурных перестроек (ПГТ-СП) направлено на обнаружение структурных изменений в хромосомах, таких как транслокации или инверсии, которые могут привести к генетическим патологиям у будущего ребенка. Примером может служить выявление инверсий при гемофилии А.
Генетическое тестирование при ЭКО — это важный инструмент в современной репродуктивной медицине, который помогает снизить риск передачи наследственных заболеваний и выкидышей. Он дает будущим родителям возможность принимать осознанные решения и планировать рождение здорового ребенка.
Гемофилии А и В: что нужно знать о генетической диагностике этих заболеваний?
Гемофилии А и В — это наследственные заболевания, при которых в организме отсутствуют или сильно снижены уровни определенных белков, участвующих в свертывании крови. В основе гемофилии А лежит дефицит фактора VIII, а гемофилии В — дефицит фактора IX. Эти белки играют важнейшую роль в каскаде свертывания крови, и их недостаток приводит к проблемам с остановкой кровотечений, что может вызывать частые и иногда опасные для жизни кровотечения. Гемофилия А встречается с частотой 1:5000 мальчиков, тогда как гемофилия В — 1:30000.
Оба типа гемофилии относятся к Х-сцепленным рецессивным заболеваниям, что означает, что ген, ответственный за выработку факторов свертывания, расположен на Х-хромосоме. Мужчины, имеющие только одну Х-хромосому, болеют гемофилией, если наследуют мутантный ген. У женщин же, благодаря двум Х-хромосомам, болезнь проявляется только если обе они несут мутацию, или если здоровая Х-хромосома по каким-то причинам не функционирует. Женщины чаще всего являются бессимптомными носителями, передавая мутацию следующим поколениям. Дочери мужчины с гемофилией всегда будут носителями, тогда как сыновья будут здоровыми. От женщины-носительницы дети унаследуют ген с мутацией с вероятностью 50%. Также мутация может возникнуть спонтанно в половой клетке одного из родителей.
Тяжесть гемофилии зависит от степени повреждения гена. Чем сильнее дефект, тем ниже активность фактора свертывания. В норме уровень активности фактора составляет более 50%, а при тяжелой форме гемофилии активность падает ниже 1%, что приводит к частым спонтанным кровотечениям, особенно в мышцы и суставы. Самые уязвимые суставы – коленные, локтевые и голеностопные. Средняя форма заболевания проявляется при активности 1-5% и обычно сопровождается кровотечениями после травм или операций, хотя спонтанные кровотечения тоже возможны. При легкой форме (активность более 5%) заболевание может протекать почти бессимптомно с кровотечениями, возникающими только при серьезных травмах или операциях.
Хотя диагноз гемофилии чаще всего ставят на основании семейного анамнеза, физического осмотра и лабораторных анализов, при легких формах заболевания для уточнения диагноза может потребоваться генетическая диагностика.
Основное назначение генетического тестирования при гемофилии — это определение носительства мутации у женщин из семей, где уже есть случаи заболевания. Это важно для планирования семьи и прогнозирования риска рождения больного ребенка. Женщинам-носительницам мутации рекомендуется пренатальная диагностика или экстракорпоральное оплодотворение с преимплантационным генетическим тестированием, чтобы предотвратить передачу заболевания будущему поколению.
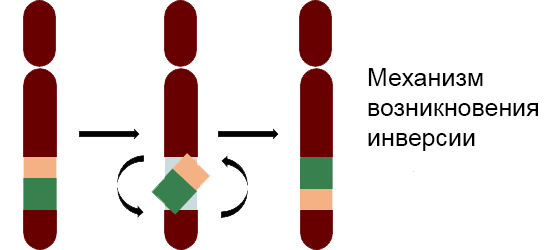
При тяжелой форме гемофилии А часто встречаются две распространенные мутации: инверсия 22 (в 50% случаев) и инверсия 1 (до 5%). Инверсии — это особый тип генетического нарушения, при котором крупный фрагмент ДНК переворачивается на 180 градусов и встраивается обратно. Поскольку при тяжелой форме гемофилии А инверсии часто встречаются, поиск мутаций обычно начинают с них. Чаще всего диагностика распространенных инверсий при гемофилии А представляет собой отдельный вид исследования в медицинских центрах.
Если инверсии исключены, выполняют поиск других видов нарушений, изучая последовательность гена F8 методом секвенирования по Сэнгеру или высокопроизводительным секвенированием.
Для гемофилии В инверсии не описаны, выполняют поиск мутаций, изучая последовательность гена F9 методом секвенирования по Сэнгеру или высокопроизводительным секвенированием.
Болезнь Виллебранда: самая частая коагулопатия
Болезнь Виллебранда — одно из самых распространённых наследственных нарушений свертываемости крови, встречающееся примерно у 1 из 10 000 человек. Это заболевание связано с дефицитом или нарушением функции фактора Виллебранда — белка, который играет ключевую роль в начальных стадиях свертывания крови. Фактор Виллебранда помогает тромбоцитам прикрепляться к месту повреждения сосудов и защищает фактор свертывания крови VIII от разрушения.
Симптомы болезни Виллебранда могут значительно варьироваться по тяжести. Наиболее частыми проявлениями являются частые и трудно останавливаемые носовые кровотечения, лёгкое появление синяков, кровотечения из дёсен и слизистых оболочек желудочно-кишечного тракта, продолжительные кровотечения после операций или стоматологических процедур, а также длительные и обильные менструации у женщин. В самых тяжёлых случаях могут возникать спонтанные обширные кровоизлияния под кожей, и при хирургических вмешательствах существует высокий риск опасных для жизни кровотечений.
Болезнь Виллебранда подразделяется на три основные типа:
-
Тип 1 — самый распространённый и лёгкий тип, при котором уровень фактора Виллебранда снижен, но его функция остаётся нормальной.
-
Тип 2 — характеризуется нарушением функции фактора Виллебранда и включает несколько подтипов (2A, 2B, 2M, 2N), каждый из которых имеет свои особенности.
-
Тип 3 — редкий и наиболее тяжёлый тип, при котором фактор Виллебранда практически отсутствует.
Типы 1 и 2A, 2B и 2M наследуются по аутосомно-доминантному типу, что означает, что для проявления заболевания достаточно одной копии мутантного гена. В этом случае один из родителей, как правило, также болен и передаёт заболевание ребёнку с вероятностью 50%, или мутация может возникнуть спонтанно. Типы 3 и 2N наследуется по аутосомно-рецессивному типу, то есть заболевание проявляется только при наличии двух копий мутантного гена — по одной от каждого родителя, которые при этом могут быть бессимптомными носителями. Вероятность рождения ребёнка с этим типом заболевания у двух носителей составляет 25%.
Болезнь Виллебранда часто подозревают у пациентов с необъяснимыми кровотечениями, особенно если в семье уже были зарегистрированы случаи этого заболевания. Диагноз ставят на основе семейного анамнеза, клинических проявлений и результатов лабораторных тестов. Иногда клиническая картина болезни Виллебранда и лёгкой формы гемофилии А может быть схожей, и тогда для точной диагностики требуется генетическое тестирование.
Генетическое тестирование может использоваться для подтверждения диагноза или для определения типа/подтипа болезни Виллебранда. Выполняется оно методом секвенирования по Сэнгеру или высокопроизводительного секвенирования гена VWF.
Талассемии: разнообразие и генетическая диагностика
Талассемия — это группа наследственных заболеваний крови, которые характеризуются нарушением синтеза гемоглобина, белка, который отвечает за транспорт кислорода по всему организму. Основное проявление талассемии — анемия. В зависимости от того, какая часть гемоглобина нарушена, различают несколько видов этого заболевания.
Гемоглобин состоит из четырёх белковых цепей: двух α-цепей и двух β-цепей. Когда нарушен синтез α-цепей, говорят об альфа-талассемии, а если нарушен синтез β-цепей — о бета-талассемии. Наиболее распространённой формой является бета-талассемия. Другие варианты заболевания встречаются крайне редко и в данной статье не рассматриваются.
Бета-талассемия бывает трёх форм:
-
Малая талассемия проявляется лёгкой анемией или даже отсутствием симптомов. Люди с этой формой имеют одну повреждённую копию гена и являются носителями заболевания.
-
Большая талассемия — самая тяжёлая форма, требующая регулярных переливаний крови и постоянного медицинского наблюдения. Она возникает, когда оба родителя передают ребёнку серьёзные мутации. При этом сами родители часто являются носителями и не испытывают выраженных симптомов. Вероятность рождения ребёнка с тяжёлой формой составляет 25% у двух носителей. Семьям, где уже были зафиксированы случаи рождения детей с тяжелыми формами талассемии, рекомендуется консультация врача-генетика.
-
Промежуточная форма имеет более лёгкое течение по сравнению с большой талассемией, и обычно не требует частых переливаний крови. Симптомы варьируются, но анемия при этой форме умеренной тяжести. Промежуточная форма развивается в случае, когда ребенок получает от родителей две копии гена с мутациями, но в этом случае нарушения в гене менее серьезные.
Бета-талассемия встречается как у мужчин, так и у женщин с частотой около 1 на 100 000 человек. Больше всего случаев заболевания наблюдается среди жителей стран Средиземноморья, Центральной и Южной Азии. В России большая талассемия редко встречается, и большинство больных — потомки выходцев из Поволжья, Кавказа или Средней Азии.
Клинические проявления талассемии включают бледность, одышку, усталость при физической нагрузке, снижение аппетита. В тяжёлых случаях симптомы могут появляться уже в раннем возрасте, у детей наблюдается задержка роста, боли в животе из-за увеличения селезёнки, желтуха, увеличение печени, деформации костей черепа, а также проблемы с сердцем.
Диагноз талассемии часто ставят с помощью электрофореза гемоглобина и лабораторных тестов крови. Для подтверждения диагноза, а также для выявления носителей без выраженной клинической картины, используется генетическое тестирование. Оно особенно важно для планирования семьи и прогноза риска передачи заболевания детям. В семьях, где оба родителя являются носителями, рекомендуется пренатальная диагностика на 10-12 неделе беременности (биопсия хориона) или на 15-20 неделе (амниоцентез), чтобы узнать о наличии мутаций у будущего ребёнка.
Альфа-талассемия, как правило, развивается в результате выпадения крупных участков генов HBA1 и HBA2, что диагностируется методом MLPA. Для выявления более редких точечных мутаций используют секвенирование по Сэнгеру. В случае бета-талассемии и аномальных гемоглобинов чаще всего причиной являются мелкие нарушения в структуре гена HBB, поэтому основным методом является секвенирование по Сэнгеру этого гена.
Порфирии: редкие, но важные заболевания
Порфирии — это группа редких заболеваний, связанных с нарушением синтеза гема — важного компонента гемоглобина и некоторых других белков. Все порфирии, кроме одной, являются наследственными. Синтез гема проходит в восемь последовательных стадий, на каждой из которых работает свой фермент. Нарушение на любой стадии — будь то избыток первого фермента или недостаток одного из следующих семи — вызывает один из восьми видов порфирий. Причиной проблем с ферментами является повреждение гена (мутация), который отвечает за выработку конкретного фермента. Из-за этого накапливаются токсичные вещества, образующиеся на предыдущих стадиях синтеза гема, что вызывает симптомы, такие как боли в животе, светочувствительность кожи, мышечная слабость и судороги.
Четыре вида порфирий (острая перемежающаяся порфирия, наследственная копропорфирия, вариегатная порфирия и врожденная поздняя кожная порфирия) передаются по аутосомно-доминантному типу. Это значит, что для проявления болезни достаточно одной копии гена с мутацией. Мутация может быть унаследована от родителя с 50% вероятностью или возникнуть спонтанно. Три других вида (дефицит дегидратазы δ-аминолевулиновой кислоты, конгенитальная эритропоэтическая порфирия, эритропоэтическая протопорфирия) наследуются по аутосомно-рецессивному типу. Болезнь проявляется только если обе копии гена содержат мутацию, при этом родители являются бессимптомными носителями, и риск рождения больного ребенка у таких родителей составляет 25%.
Х-сцепленная протопорфирия передается по Х-сцепленному доминантному типу. Это означает, что заболевание может проявляться как у женщин, так и у мужчин, если хотя бы одна из Х-хромосом содержит мутацию. Мужчины с этим заболеванием передают его только дочерям, так как передача по мужской линии невозможна.
Порфирии делятся на острые и кожные в зависимости от симптомов. Острые порфирии проявляются приступами сильной боли, чаще всего в животе, а также психическими нарушениями (тревога, депрессия) и неврологическими симптомами (слабость, паралич, судороги). Кожные порфирии вызывают светочувствительность, которая приводит к образованию пузырей и язв на коже. Некоторые порфирии, например наследственная копропорфирия или вариегатная порфирия, могут сочетать как кожные, так и острые проявления.
Самой распространённой формой является острая перемежающаяся порфирия, причиной которой служат мутации в гене HMBS.
Диагностика порфирий основана на анализе уровня токсичных предшественников гема, что помогает определить тип порфирии, но, к сожалению, этот метод эффективен только во время приступов. Единственным точным методом диагностики остаётся генетическое тестирование, которое можно проводить в любое время. Оно остается информативным и вне приступа. Тестирование выполняется методом секвенирования по Сэнгеру тех генов, мутации в которых связаны с порфириями.
Порфирии характеризуются неполной пенетрантностью, что означает, что не у всех людей с мутацией развиваются симптомы. Однако определенные факторы, такие как определенные лекарства, инфекции, гормональные изменения или диета, могут спровоцировать приступ порфирии у людей с мутацией. Это в значительной степени осложняет диагностику и лечение порфирий. Генетическое тестирование членов семей больных позволяет выявить носителей мутаций без симптомов и предупредить их о возможных триггерах, чтобы снизить риск проявления болезни.