Первый пациент, который был включен в клиническое исследование первого отечественного CAR-T-клеточного препарата «Утжефра», завершил первый этап лечения без осложнений и перешел на амбулаторный режим для оценки работы препарата в долгосрочной перспективе.
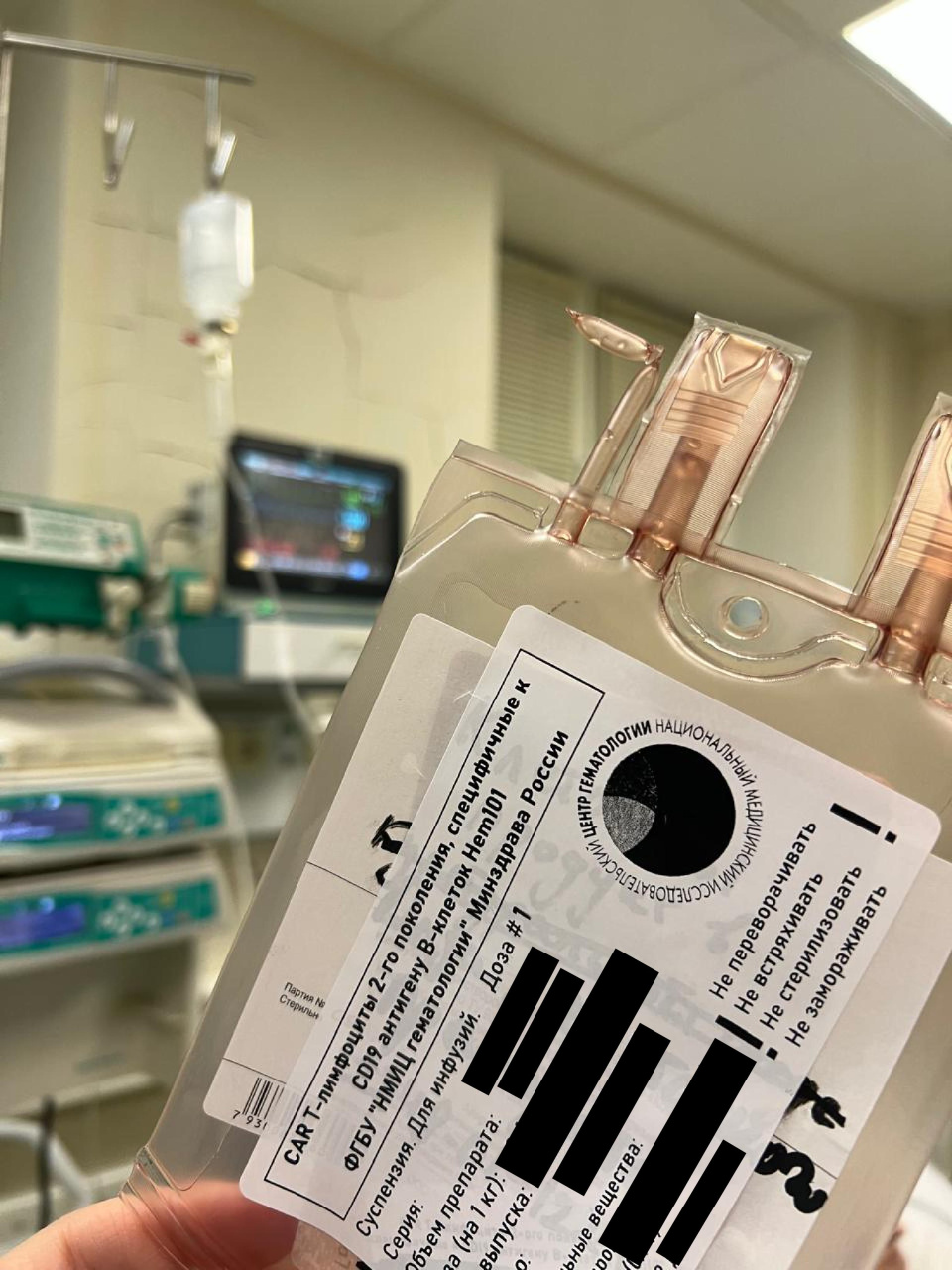 Первое в России клиническое исследование отечественного CAR-T-клеточного препарата «Утжефра» для лечения злокачественных заболеваний крови началось в НМИЦ гематологии Минздрава России в декабре 2024 года. В клиническое исследование включаются пациенты с рецидивами или рефактерными формами B-клеточных злокачественных новообразований крови. Главное условие включения — присутствие на поверхности опухолевых клеток антигена CD19.
Первое в России клиническое исследование отечественного CAR-T-клеточного препарата «Утжефра» для лечения злокачественных заболеваний крови началось в НМИЦ гематологии Минздрава России в декабре 2024 года. В клиническое исследование включаются пациенты с рецидивами или рефактерными формами B-клеточных злокачественных новообразований крови. Главное условие включения — присутствие на поверхности опухолевых клеток антигена CD19.
Первый пациент, получивший экспериментальный CAR-T-клеточный препарат "Утжефра", успешно завершил участие в первой фазе клинического исследования. По результатам обследования подтвержден полный ответ на терапию и безопасность препарата. В течение года после введения препарата все пациенты будут проходить периодические осмотры, анализы крови, инструментальные исследования для определения статуса по основному заболеванию и контроля ремиссии. Все пациенты-участники исследования будут оставаться под наблюдением еще в течение 15-ти лет для оценки возможных отсроченных осложнений.
«Первый пациент-участник клинического исследования — это женщина 59 лет, она получила «Утжефру» 12 и 13 декабря двумя дозами, — рассказывает главный исследователь, заведующая отделом клеточной и иммунной терапии НМИЦ гематологии Минздрава России Ольга Алешина. — Она болеет чуть больше года. Первоначально пациентка обратилась на амбулаторный прием в наш центр, где был уточнен диагноз, а также обнаружена мутация, определяющая неблагоприятный прогноз заболевания. Пациентке была проведена блоковая терапия с высокими дозами цитостатиков, затем она находилась на поддерживающем лечении, однако через некоторое время произошел рецидив, то есть возврат заболевания. Учитывая неблагоприятный прогноз и отсутствие ответа на лечение, пациентка была рассмотрена как кандидат на включение в клиническое исследование. После введения «Утжефры» у пациентки не было серьезных осложнений, через неделю наблюдения в отделении реанимации и интенсивной терапии, что предусмотрено протоколом исследования, она была переведена в гематологическое отделение и далее наблюдалась в условиях дневного стационара. Мы отслеживаем показатели крови, работу CAR-T-клеток, состояние жизненно важных органов».
 В исследовании примут участие 60 пациентов. Пациенты включаются в клиническое исследование на основании решения врачебной комиссии НМИЦ гематологии Минздрава России с учетом жесткого соблюдения всех критериев, в том числе наличия антигена CD19 на опухолевых клетках. Далее проверяются другие критерии — соматический статус, состояние всех органов и систем, количество Т-клеток в периферической крови. Это важные критерии, так как препарат производится из собственных Т-клеток пациента.
В исследовании примут участие 60 пациентов. Пациенты включаются в клиническое исследование на основании решения врачебной комиссии НМИЦ гематологии Минздрава России с учетом жесткого соблюдения всех критериев, в том числе наличия антигена CD19 на опухолевых клетках. Далее проверяются другие критерии — соматический статус, состояние всех органов и систем, количество Т-клеток в периферической крови. Это важные критерии, так как препарат производится из собственных Т-клеток пациента.
CAR-T-клеточный препарат «Утжефра» для лечения В-клеточных злокачественных новообразований крови разработан в лаборатории трансплантационной иммунологии НМИЦ гематологии Минздрава России и прошел все фазы доклинических исследований.
«Маленькие победы на пути к большой цели делают ее выполнимой, — говорит заведующая лабораторией трансплантационной иммунологии НМИЦ гематологии Минздрава России Аполлинария Боголюбова-Кузнецова. — На первых этапах разработки мы смотрели как именно препарат работает с опухолевыми клетками, подбирали оптимальные условия его получения. Теперь дело за производством, отделом технологического контроля, врачами и средним медицинским персоналом. Эти маленькие шаги постепенно приведут нас к итоговой цели — получению работающего CAR-T-клеточного препарата, доступного широкому кругу пациентов».
«Утжефра» (непатентованное название — гемагенлеклейцел) предназначена для лечения В-клеточных злокачественных новообразований, несущих на своей поверхности антиген CD19. В ходе клинических исследований оценивается переносимость, безопасность и эффективность препарата у взрослых пациентов с рецидивами и рефрактерными формами таких заболеваний.
Ранее по теме:
Началось первое клиническое исследование отечественного CAR-T-клеточного препарата
Получение лицензии Минпромторга России


